O Ministério da Saúde anunciou neste sábado (27) uma
parceria para a pesquisa e produção nacional da vacina contra a Covid-19
desenvolvida pela Universidade de Oxford, do Reino Unido, e a farmacêutica
AstraZeneca.
O acordo prevê a transferência de tecnologia e a compra de
lotes da vacina. Se for comprovada a eficácia da imunização, ao menos 30,4
milhões de doses serão entregues em dois lotes: 15,2 milhões em dezembro de
2020, e 15,2 milhões em janeiro de 2021, com prioridade para o grupo de risco e
para profissionais de saúde.
Após as primeiras duas entregas, segundo o ministério, ainda
poderão ser produzidas mais 70 milhões de doses para distribuição a partir do
Sistema Único de Saúde (SUS).
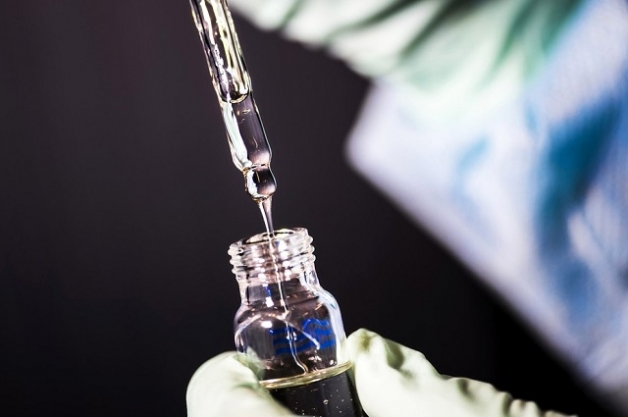
"Nesse primeiro momento, o IFA (ingrediente
farmacêutico ativo) vem pronto (do exterior)", explicou o secretário de
Ciência, Tecnologia e Insumos Estratégicos, Hélio Angotti Neto. "Ele vai
ser processado e distribuído para a população brasileira."
Angotti reforçou que há, no acordo, o orçamento de
importação de mais IFA para a ampliação da produção nacional. Segundo ele, a
compra de mais princípios ativos será feita após uma reavaliação do mercado
internacional. Ele disse também que é possível que surja outras opções
concorrentes de vacina.
No Brasil, a tecnologia será desenvolvida pela Fundação
Oswaldo Cruz (Fiocruz), que será preparada para fabricar a imunização
distribuída no país com a tecnologia estrangeira.
Em um comunicado, a pasta formalizou que governo federal
aceitou uma proposta feita pela embaixada britânica e a farmacêutica para a
cooperação no desenvolvimento tecnológico e acesso do Brasil à vacina
ChAdOx1.
Acordo em duas etapas
O acordo tem duas etapas, diz o ministério. A primeira,
consiste na encomenda de frascos da imunização e também que o país assuma os
custos de parte da pesquisa. O país se compromete a pagar pela tecnologia,
ainda que não tenham se encerrado os estudos clínicos finais.
Em uma segunda fase, caso a vacina se mostre eficaz e
segura, será ampliada a compra. Se a vacina for licenciada, a pasta estima a
compra de mais 70 milhões de doses, no valor estimado de US$ 2,30 (cerca de
R$12,60) por dose.
"Nessa fase inicial, de risco assumido, serão 30,4
milhões de doses da vacina, no valor total de U$ 127 milhões, incluídos os
custos de transferência da tecnologia e do processo produtivo da Fiocruz,
estimados em U$ 30 milhões. Os dois lotes a serem disponibilizados à Fiocruz,
de 15,2 milhões de doses cada, deverão ser entregues em dezembro de 2020 e
janeiro de 2021", diz o comunicado.
O secretário de Vigilância em Saúde, Arnaldo Correia de
Medeiros, explicou em uma entrevista coletiva que há um "risco
associado" a esta parceria.
"No desenvolvimento de uma encomenda tecnológica,
existe um risco associado a ele. Os estudos preliminares de fase 1 e 2 mostram
que tem uma resposta bastante significativa, mas se os estágios clínicos não se
mostrarem seguros, teremos aprendido com o avanço tecnológico."
Vacina de Oxford
Na sexta-feira (26), uma cientista da Organização Mundial da
Saúde (OMS), disse que a vacina testada no Brasil contra a Covid-19, que é
feita pela Universidade de Oxford e pela AstraZeneca, é a mais adiantada no
mundo e a mais avançada em termos de desenvolvimento.
Soumya Swaminathan disse também que uma outra vacina em fase
de testes – idealizada pela empresa Moderna – "não está muito atrás"
da potencial imunização da AstraZeneca. Os dois projetos estão entre as mais de
200 vacinas candidatas contra a Covid-19, das quais 15 já entraram na fase de
testes clínicos, em humanos.
A vacina ChAdOx1está na fase 3 de desenvolvimento – última
fase antes da aprovação e distribuição – e começou a ser testada nesta semana
em voluntários brasileiros, em um estudo liderado no país pela Universidade
Federal de São Paulo (Unifesp).
Etapas para a produção
Para chegar a uma vacina efetiva, os pesquisadores precisam
percorrer diversas etapas para testar segurança e resposta imune. Primeiro há
uma fase exploratória, com pesquisa e identificação de moléculas promissoras
(antígenos).
O segundo momento é de fase pré-clínica, em que ocorre a
validação da vacina em organismos vivos, usando animais (ratos, por exemplo).
Só então é chegada à fase clínica, em humanos, dividida em
três momentos:
Fase 1: avaliação preliminar com poucos voluntários adultos
monitorados de perto;
Fase 2: testes em centenas de participantes que indicam
informações sobre doses e horários que serão usados na fase 3. Pacientes são
escolhidos de forma randomizada (aleatória) e são bem controlados;
Fase 3: ensaio em larga escala (com milhares de indivíduos)
que precisa fornecer uma avaliação definitiva da eficácia/segurança e prever
eventos adversos; só então há um registro sanitário – G1.
Carlos Magno
VEJA TAMBÉM:
- Cheirar pum pode prevenir câncer, AVC,
ataque cardíaco, artrite e demência, diz estudo de universidade do Reino Unido
- Assassinato de moradores de rua em
Campina Grande-PB gera comoção: radialista faz artigo em homenagem a
"Maria Suvacão"
- UEPB vai ganhar curso de Medicina no campus de
Campina Grande. Veja detalhes
-Cliente que passar mais de 20 minutos em fila de
banco na Paraíba receberá indenização
- Jovem forja a própria morte para saber
"quais pessoas se importariam com sua ausência" e vem a público pedir
desculpas