O governo de São Paulo anuncia nesta segunda-feira, 19, que
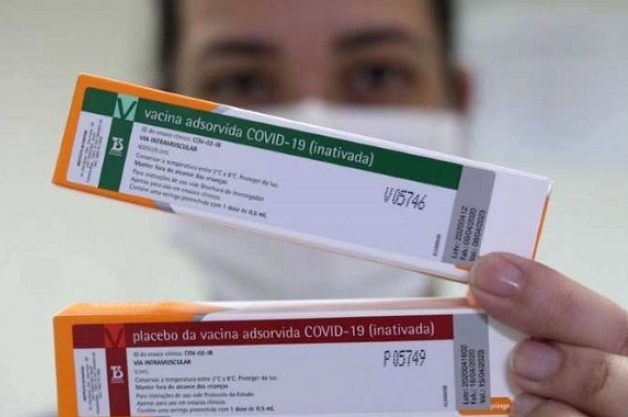
a vacina Coronavac, desenvolvida pelo Instituto Butantã em parceria com a
farmacêutica chinesa Sinovac, se mostrou segura também em testes com 9 mil
voluntários brasileiros, reafirmando os resultados de pesquisa anterior com 50
mil participantes chineses. Os dados de eficácia, porém, devem ser divulgados
somente entre novembro e dezembro, o que deve atrasar a previsão do governador
João Doria (PSDB) de iniciar a imunização ainda neste ano.
De acordo com Dimas Covas, diretor do Butantã, os testes com
os 13 mil voluntários não foram finalizados e a análise de eficácia ainda não
pode ser feita. O pesquisador afirmou que foi concluída nesta semana só a
primeira etapa do estudo, com 9 mil pessoas. Mesmo nesse grupo, nem todos
tomaram as duas doses ainda, o que deve ocorrer até o fim do mês. “Já temos os
dados de segurança dessa etapa, eles são muito parecidos com os chineses
(estudo em que mais de 90% dos voluntários não tiveram eventos adversos).
"São esses dados que vou detalhar na segunda. Eficácia
ainda não dá para falar porque temos de esperar as pessoas terem contato com o
vírus. Pela minha impressão, acho que teremos dados conclusivos mais para o fim
do ano, entre novembro e dezembro”, disse ao Estadão.
Eficácia da vacina
Covas explicou que as conclusões sobre eficácia dependem da
ocorrência de um número mínimo de infecções por covid-19 entre os voluntários.
Esse índice, definido por cálculos estatísticos, é necessário para que os
pesquisadores comparem quantos dos contaminados estavam no grupo vacinado e
quantos faziam parte do grupo que recebeu o placebo. Se o total no segundo
grupo for significativamente superior ao do primeiro, haverá evidência de que a
vacina foi capaz de proteger contra a covid.
No caso do estudo da Coronavac, o número mínimo para uma
primeira análise é de 61 contaminados, o que, de acordo com o diretor do
Butantã, ainda não foi atingido. “Esse é o número necessário para que possamos
fazer a análise interina (tipo de avaliação feita antes da conclusão da
pesquisa). Se com 61 casos não for possível demonstrar a eficácia, vamos
esperar ter 151 casos. Aí certamente conseguiremos concluir.”
Com resultados de eficácia esperados somente para novembro
ou dezembro, é improvável que o início da vacinação aconteça ainda em 2020 não
só pelo tempo que falta para os testes serem concluídos, mas também pelo prazo
para que a Agência Nacional de Vigilância Sanitária (Anvisa) analise as
informações e emita o registro do produto.
A análise da vacina
Embora o órgão tenha criado um novo fluxo de análise, que
permite aos pesquisadores enviarem de forma contínua os dados da pesquisa assim
que eles são produzidos, só informações das fases pré-clínicas (testes feitos
em laboratório ou animais) da Coronavac já estão com a agência, como afirmou ao
Estadão Gustavo Mendes, gerente geral de medicamentos da Anvisa. “Ainda não
recebemos os dados de fase 1 e 2, por exemplo, mas alguns pesquisadores
preferem enviar os dados de todas as fases clínicas de uma vez só”, afirmou.
Ele conta que, mesmo diante de um momento de emergência como
o da pandemia, a análise dos estudos precisa seguir alguns trâmites e destaca
que análises interinas nem sempre apresentam dados suficientes para a liberação
do registro. “A grande questão da análise interina é que, dependendo do
porcentual de voluntários infectados, ela pode não ter um poder estatístico
para confirmar a eficácia. Para subsidiar registro, a análise interina precisa
ter evidência muito robusta”, explica.
Mendes destaca que o prazo máximo para a agência avaliar um
pedido de registro de um medicamento ou vacina contra covid é menor do que o
adotado para situações normais – dois meses, ante um ano. Mas a análise não é
simples. “Um pedido de registro inclui aproximadamente 10 mil páginas de
documentos. A gente avalia informações de eficácia e segurança, mas também de
qualidade da produção. Precisamos emitir uma certificação para a fábrica na
China que vai produzir as doses”, detalha.
Por causa da pandemia, a agência reviu suas regras também
quanto à eficácia mínima exigida para a concessão do registro para a vacina.
Geralmente, imunizantes só são aprovados se conferirem a partir de 70% de
proteção. Para vacinas contra covid, a Anvisa já admite que poderá conceder a
licença com 50%.
Caso a Coronavac seja aprovada, já há acordo entre o governo
paulista e a farmacêutica chinesa para o fornecimento de 46 milhões de doses
ainda este ano.
Presidente da Sociedade Brasileira de Imunologia, Ricardo
Gazzinelli defende que haja um tempo maior de seguimento dos voluntários antes
de ser solicitado o registro. “O ideal é que fossem pelo menos dez meses para
medir eficácia”, afirma – Estadão.
Carlos Magno
VEJA TAMBÉM:
- Cheirar pum pode prevenir câncer, AVC,
ataque cardíaco, artrite e demência, diz estudo de universidade do Reino Unido
- Assassinato de moradores de rua em
Campina Grande-PB gera comoção: radialista faz artigo em homenagem a
"Maria Suvacão"
- UEPB vai ganhar curso de Medicina no campus de
Campina Grande. Veja detalhes
-Cliente que passar mais de 20 minutos em fila de
banco na Paraíba receberá indenização
- Jovem forja a própria morte para saber
"quais pessoas se importariam com sua ausência" e vem a público pedir
desculpas